衡水金卷先享题2026年夯基卷地理HJ2试卷,分学科专项试卷,精准匹配学科需求,备考更具针对性!解析附带解题多种思路,拓宽思维角度,灵活解题有方法!
11.(20分)(1)HA=H++A(3分)(2)6(3分)(3)>(2分)(4)①b=c>a(3分)②<(2分)(5)NH₄Cl(2分)>(2分)(6)①>②>③(3分)
【解析】(1)HA溶液中含有两种电中性分子,说明HA为弱酸,则HA的电离方程式为HA一H+A-。
(2)某温度下,0.1 mol·L-¹的盐酸中氢离子浓度为0.1mol·L-¹,水电离出的c(H+)=1.0×10-¹¹mol·L-¹,溶液中的氢氧根离子来自水的电离,c(OH-)水=c(H+)水=1.0×10⁻¹¹mol·L-¹.则该温度下的水的离子积常数为1.0×10⁻¹²;pH=11的Ba(OH)₂溶液中的c(OH-)与pH=1的H₂SO₄溶液中的c(H+)均为0.1mol·L-¹,两者等体积混合恰好完全中和,最终溶液呈中性.pH=6。(3)10 mL 0.1 mol·L-¹的NaOH溶液与10 mL0.2 mol·L-¹的HF溶液混合后,NaF和HF的浓度比为1:1,溶液显酸性,说明HF电离大于NaF水解,则有
K。(HF)>Ks(NaF)=K
、K(HF)>√K。(4)①酸抑制水电离,酸中c(HT)越大,水电离程度越小,c(H+):a>b=c.所以水电离程度:b=c>a。②pH相同的HA、HB溶液分别加水稀释相同的倍数,pH值变化较大的酸.其酸性较强,根据图知:lg。2时,溶液稀释100倍,HA溶液的pH增大2,说明HA是强酸;HB溶液pH值增大数值小于2,说明稀释过程中HB继续电离,则HB为弱酸;常温下,取上述pH均为3的HA和HB溶液各
100 mL,c(HA)<c(HB),则n(HA)<n(HB),则n1<n2。
(5)分别加热到50℃,盐酸溶液中氢离子浓度变化不大·氯化铵溶液中水解是吸热反应,加热促进水解,氢离子浓度增大,溶液pH较小的是NH₄Cl溶液;加水稀释至50 mL,稀释10倍,促进氯化铵中铵根离子水解,则c(H+)>10⁻⁶mol·L-¹。
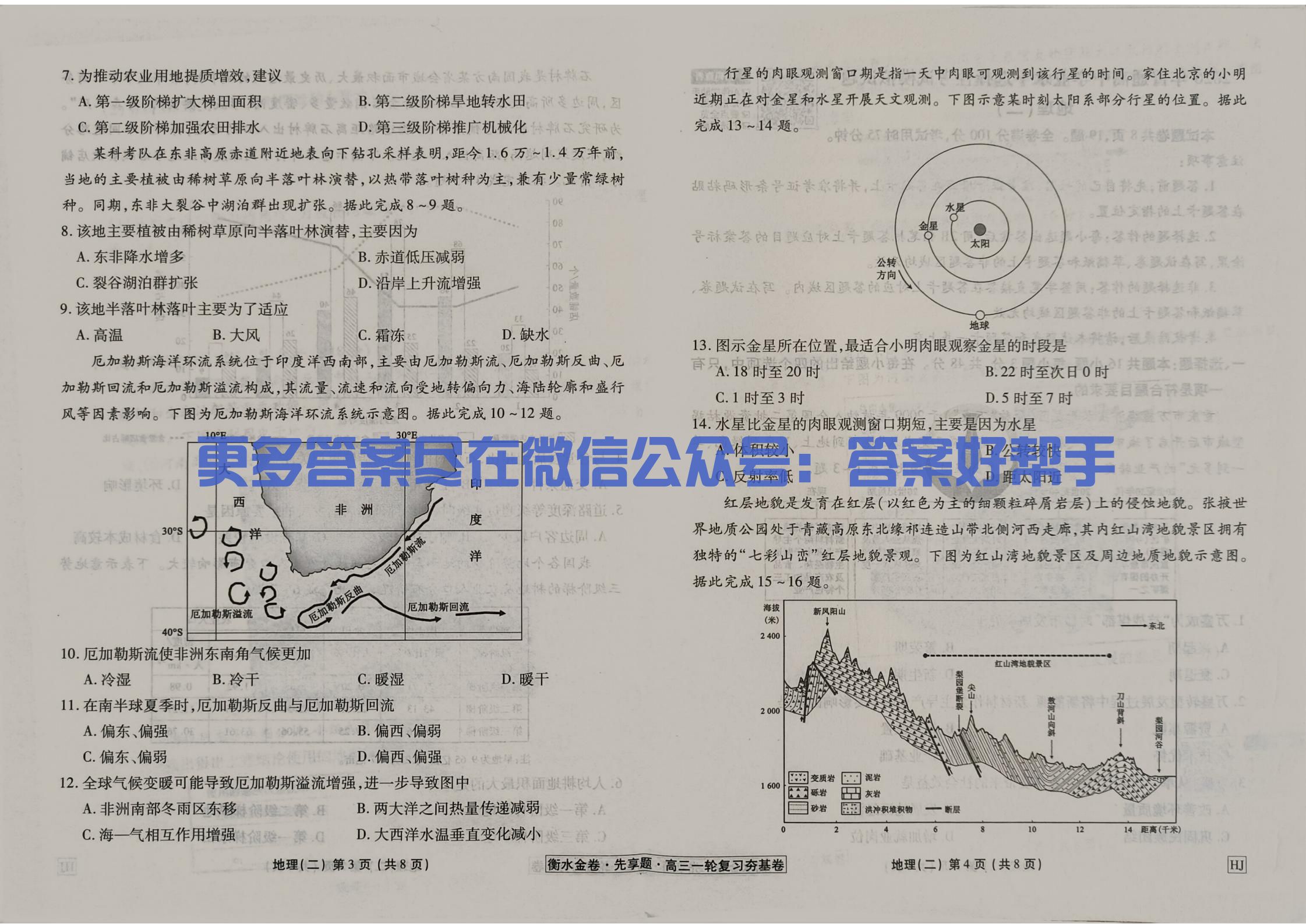
(6)根据“越弱越水解”,得到碳酸钠水解程度最大,次氯酸钠水解程度次之,氟化钠水解程度最小,由于三者水解出的氢氧根浓度相同,则水解程度越大,说明其物质的量浓度越小,因此常温下,pH相同的三种溶液①NaF溶液;②NaClO溶液;③Na₂CO₃溶液,其物质的量浓度由大到小的顺序是①>②>③。
衡水金卷先享题2026年夯基卷地理HJ2试卷,解析附带解题多种思路,拓宽思维角度,灵活解题有方法!分学科专项试卷,精准匹配学科需求,备考更具针对性!